摘要:以西番莲果皮为原料,利用超声辅助提取法提取原花青素(PC),并对西番莲果皮PC进行纯化及对亚硝化的抑制作用进行讨论。固定提取条件,研究AB-8大孔树脂对PC的纯化效果。用纯化后的原花青素进行二甲基亚硝胺合成的阻断实验,发现最大阻断率为88.4%。同时,探究原花青素对NaNO2清除率的浓度梯度试验,得到最大清除率为84.1%。表明相同浓度的PC对亚硝胺的阻断更强,证明其有抑制亚硝化反应的能力。
关键词:提取;西番莲;亚硝化
据统计,全球每年有500多万癌症患者,我国癌症率也非常高。身边的人也有出现患有癌症的病人,他们忍受着巨大的疼痛和痛苦。常见的强致癌性物质中就包括N-亚硝基化合物,而亚硝胺和亚硝酰胺都属于N-亚硝基化合物,在反应生成之前,它的前体物质为亚胺和亚硝酸盐。研究者不仅会根据食品中亚硝酸盐的含量判定其是否适宜食用[1-4],还会研究用某种物质降低食品中亚硝酸盐的含量,阻止合成有毒致癌性物质亚硝胺,减轻对人体的伤害。现代药理研究表明多酚类化合物具有多种生物活性,显示抗肿瘤、抗衰老、增强免疫力等药理作用[1]。
原花青素(Procyanidins,PC),广泛存在于自然植物中,是由黄烷-3-醇为单体缩合而成的多酚类物质,具有极强的抗氧化活性和消除自由基的作用[5,6],其抗自由基的氧化能力是维生素C的20倍、维生素E的50倍[7]。本实验以百香果(又叫鸡蛋果或西番莲)果皮为原料,利用超声辅助提取法提取原花青素,且用AB-8对果皮原花青素进行纯化,再对亚硝化的抑制作用进行讨论,为百香果原花青素的深度开发和综合利用提供科学依据[8,9]。
1材料与方法
1.1 PC提取:保山本地西番莲果皮干燥后粉碎,过60筛目后采用超声辅助溶剂法提取PC。
1.2 AB-8对PC的静态吸附和解吸实验:准确称取1g处理好的AB-8分别置于6个100mL具塞锥形瓶中,然后加提取液30mL,用保鲜膜将口密封,放入摇床振荡器中振荡,每隔10min测定一次吸光度,记录所测吸光度值,计算其吸附率。然后将吸附后的AB-8抽滤后置于100mL具塞锥形瓶中,用40mL50%乙醇溶液,在恒温25℃,转速为120r/min振荡器中振荡洗脱,每隔10分钟测定一次吸光度,计算解吸率。
1.3 PC对亚硝胺阻断率的测定
吸取一系列原花青素提取液置于25mL容量瓶中,取pH=3的柠檬酸钠-盐酸缓冲液10mL,依次加1mmol/L的NaNO21mL,1mmol/L的二甲胺,将反应体系定容至25mL,最后放置在37℃水浴下恒温1h。用移液管吸取1.0mL该溶液加到7cm2的培养皿中,加入0.5%的NaCO3溶液0.5mL,紫外灯照射15min,取出后加1%对氨基苯磺酸溶液1.5mL,0.1%的α-萘胺1.5mL,摇匀放置15min后,于525nm处测吸光度值(AX)。同时用乙醇溶液做空白实验(A0),根据A计算阻断率。如式(1)所示。
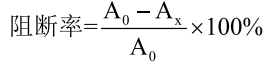
(1)
1.4 PC对NaNO2清除率的测定按照1.3定容恒温后将原花青素提取液置于培养皿中,加0.4%的对氨基苯磺酸溶液2mL,0.2%的N-1-萘乙二胺盐酸盐溶液2mL,摇匀放置15min后,根据吸光度值计算清除率,如式(2)。
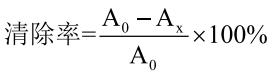
(2)
2结果与分析
2.1AB-8对PC的纯化的讨论
2.1.1 PC的静态吸附及其吸附动力学
采用1.2的方法,以吸附时间为纵坐标,吸附率为横坐标得到吸附曲线如图2-1所示。
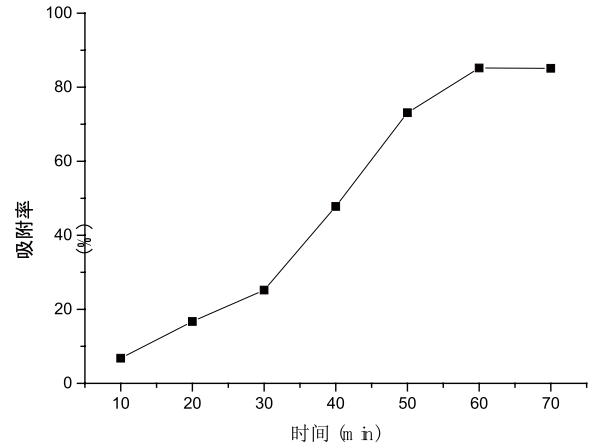
2-1静态吸附曲线
通过静态吸附动力学曲线图可以看出,随着时间的增加,AB-8吸附率不断的增加。当吸附60min时,吸附率达85.2%,最大。继续增加吸附时间,吸附率基本不变,证明已达吸附平衡。影响吸附率的因素可能有:吸附剂的性质(吸附剂本身的性质将影响吸附量及吸附速度),吸附的表面积和孔隙,吸附剂的极性也影响物质的吸附量。
2.1.2 PC的静态解吸及其解吸动力学
将吸附了PC的大孔树脂进行抽滤后加入40mL50%的乙醇进行洗脱,绘制静态解吸动力学曲线如图2-2所示。
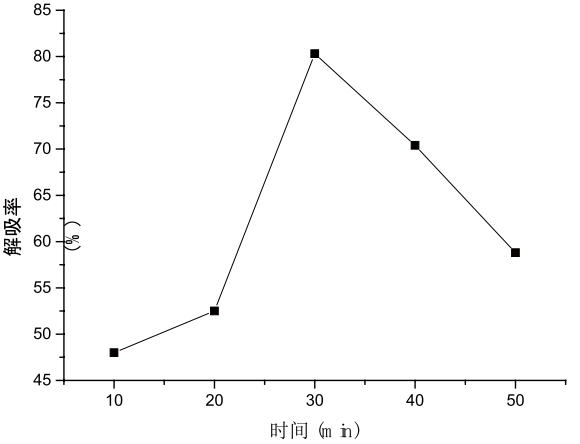
2-2 静态解吸曲线
由图可知,解吸率随着时间的增加先增大再减小,在30min时达到最大值,此时解吸率为80.3%。在30min后又呈下降趋势,随着时间的增加,解吸率降低。即百香果果皮中PC静态解吸的最佳时间为30min左右。影响解析的因素可能有:溶液的pH(往往会影响吸附剂和吸附质的解离效果);洗脱剂的影响(不同洗脱剂对其解吸的效果不同);洗脱剂的浓度也是影响其解吸效果的一个重要因素。
2.1.3料液比对纯化效果的影响称取一定量的AB-8,加PC提取液的体积不同,吸附效果也不同。以1g AB-8加入的PC体积(mL)为横坐标,吸附率为纵坐标,结果如图2-3所示。
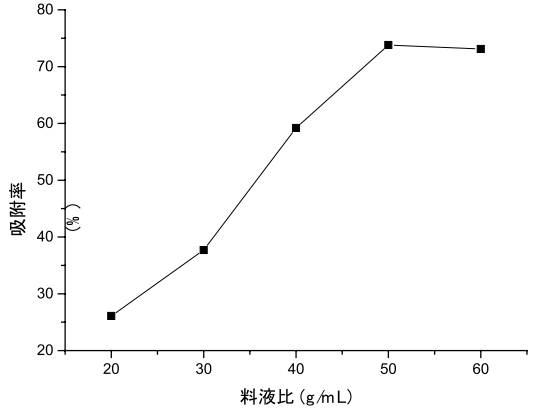
2-3 料液比对吸附率的影响
由图2-3可知,随着PC量的增加,其影响效果越明显,当加入PC的量为50mL时达到最大值,50mL以后基本趋于稳定。由此可知,当料液比为1:50(g/mL)时,AB-8对PC的吸附效果最佳。
2.1.4洗脱剂浓度对解吸率的影响
同理,洗脱剂的种类与浓度也会影响PC的溶出。分别配制浓度为40%,50%,60%,70%和80%的乙醇溶液,以一定的体积对吸附后的AB-8进行洗脱,讨论洗脱剂浓度对解吸率的影响,曲线图如图2-4所示。
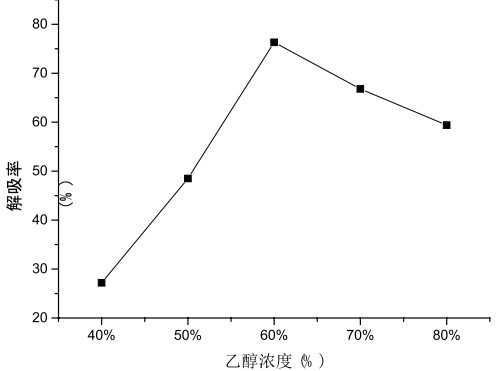
2-4 乙醇浓度对解吸率的影响
由图可知,随着乙醇浓度的增加解吸率先呈上升趋势然后呈下降趋势,在乙醇浓度为50%的时候解吸率最大,达到峰值。产生这种现象的原因可能是由于乙醇浓度很高时能溶解出一些弱极性物质。
2.2纯化后的PC对亚硝胺的阻断
将纯化后的PC进行二甲基亚硝胺(NDMA)合成的阻断实验,用亚硝胺量的多少来反映原花青素阻断能力的强弱。生成亚硝胺量少,计算得到的阻断率越高,原花青素的阻断能力就强,反之则弱。图2-5为PC对亚硝胺的阻断图。
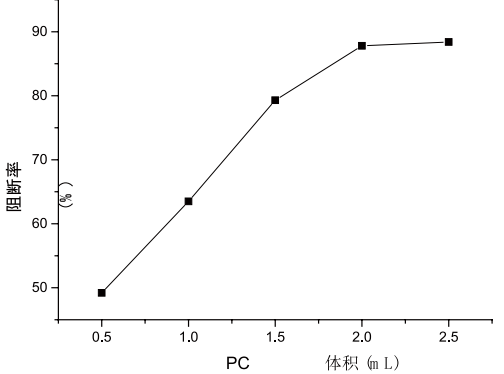
2-5 PC对亚硝胺的阻断
由图可看出,PC对亚硝胺有较强的阻断效果。随着PC量的增加,对其亚硝酸盐的阻断率越大,当PC体积为2.0-2.5 mL时趋于稳定,2.0mL时其阻断率最大,得到百香果果皮中PC对亚硝胺的最大阻断率为88.4%。
2.3纯化后PC对NaNO2的清除
按照1.4的方法,讨论PC的加入量对清除NaNO2的影响。以PC体积为横坐标,清除率为纵坐标,曲线图如图2-6所示。
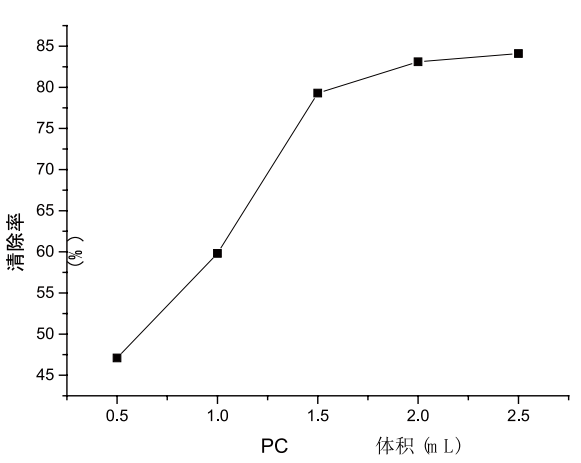
2-6 PC对NaNO2的清除
由可知,随着百香果果皮中原花青素的浓度的增加,其对亚硝酸钠的清除率先呈上升趋势后又趋于平稳,在PC体积为2.0-2.5 mL趋于稳定,2.0mL时达到最佳清除效果,最佳清除效果为84.1%。相同浓度的PC,对亚硝胺的阻断强于对NaNO2的清除。
3结论
将西番莲果皮中的PC提取物添加到亚硝化反应的过程中,显示对二甲基亚硝胺和亚硝酸盐的含量均有抑制作用,初步证明纯化后的PC能够抑制亚硝化反应的发生。但对其影响的机理,如何抑制亚硝化反应还需进一步的研究。
参考文献:
[1]张颖琦,沈俊毅,徐映如,等.亚硝酸盐对人体的危害及检测方法的进展[J].职业与健康,2015,31(6):851-855.
[2]邹华军,李鸣,杨雪峰,等.传统泡菜与乳酸菌发酵泡菜亚硝酸盐和硝酸盐含量动态变化分析[J].现代预防医学,2013,40(20):3732-3734,3739.
[3]王华,刘霞,杨继红,等.葡萄籽原花青素抗癌活性及其机制研究进展.安徽大学学报:自然科学版,2012;36(4):101-108.
[4]许钢,张虹,鹿洁.竹叶提取物对亚硝化反应抑制作用的研究[J].郑州工程学院报,2001,22(1):69-72.
[5]吴春,代丽君,聂芊.原花青素对亚硝化反应的抑制作用研究[J].天然产物研究与开发,2005(2):213-216.
[6]李绮丽,彭芳刚,刘德明,等.红莲外皮原花青素的纯化与分析[J].食品科学,2014,35(3):106-110.
[7]李莹,李才国.原花青素提取、分离纯化方法的研究进展[J].食品工程,2008,(1):9-11.
[8]李莹,李才国.原花青素提取、分离纯化方法的研究进展[J].食品工程,2008,(1):9-11.
[9]徐怀德,闫宁环,陈伟,等.黑莓原花青素超声波辅助提取优化及抗氧化性研究[J].农业工程学报,2008,42(2):264-268.